
如果實驗設計不嚴謹——以漸凍人症轉基因(yīn)小鼠藥物(wù)研發為例
肌萎縮性脊髓側索硬化(huà)症

因中(zhōng)樞神經係統內控(kòng)製骨骼肌運動的(de)神經元退化導致的肌萎縮性脊髓側索(suǒ)硬化症(Amyotrophic lateral sclerosis: ALS,也稱漸凍人症)是一種漸進(jìn)且(qiě)致命的(de)神經退行性疾病。由於運動(dòng)神經元退化和死(sǐ)亡,肌(jī)肉逐漸萎縮致大腦完全喪失(shī)控製隨意運動的能力,最終會造成發音、吞咽,以及呼吸和運動障礙。著名物理學家霍金就是一名ALS患者。目前還沒有真正可有效治療ALS的(de)藥物和方法。
絕大多數(90-95%)的ALS發病原因不明,但也有(yǒu)約(yuē)5-10%的(de)ALS患者表現出了家族遺傳性,其中超氧化物歧化酶(méi) 1(Superoxide Dismutase 1:SOD1)基因突變約占這些(xiē)遺傳性ALS病例的10%。SOD1也是第一個(gè)被鑒定出來的ALS風險基因[1],因此很快就有科學家(jiā)構建了一(yī)種含有第(dì)93位甘氨酸突變為丙氨(ān)酸(G93A)的人SOD1基因的(de)轉基因(yīn)小鼠模型,全名為B6SJL-Tg(SOD1*G93A)1Gur/J轉基因小鼠[2]。該轉基因小鼠基因(yīn)組中被轉入了23個拷貝的人源SOD1*G93A突變基因,接下來(lái)我們將其簡稱SOD1*G93A轉基因小鼠。

圖二:SOD1*G93A轉基因小鼠是(shì)以B6和SJL雜交子代為背景品係,通過原核注射和胚胎(tāi)移植得到(dào)的轉基因小鼠模型,因此其(qí)毛色多樣,圖片來自Jax實驗室(https://www.jax.org/strain/002726)
自1996年SOD1*G93A轉基(jī)因小鼠問世以後,其(qí)就被廣泛應用於ALS藥物研發的臨床前(qián)動物試驗(yàn)中。到2004年(nián),短短8年時間內,已至少有50篇文(wén)章描述了從小分子到(dào)病毒載體的各類ALS治療方案,可延長SOD1*G93A轉基因小鼠的(de)壽命,其中最長可以(yǐ)延長(zhǎng)壽命100天(78%的壽命延長)。這些藥物很快進入臨床試(shì)驗,然而,迄今為止,除了利魯唑(最多延(yán)長ALS患者兩(liǎng)個(gè)月壽命)之外,沒有任(rèn)何一種藥物顯示出對(duì)人類ALS疾病的進(jìn)程有顯著影響(xiǎng)[3]。這給醫藥公司帶來了巨(jù)大損失,如2008年在美國國家科學院院刊上發表的一篇文章顯示鋰可以將SOD1*G93A轉基因小鼠的存活時間延長30天[4]。由於鋰早已經(jīng)被用於治療精神分裂症,許多ALS患者開始超(chāo)說明書服用該藥物,希望減緩疾(jí)病進程。然而,招募了數百名患者,花費了遠超1億美元的三(sān)個同時啟(qǐ)動的獨(dú)立III期臨床試驗結果卻顯(xiǎn)示鋰對ALS無任何治療(liáo)效(xiào)果。
其實不僅僅(jǐn)是ALS的藥物研發,在整個醫藥研(yán)發領域,動物實驗結果的平(píng)均臨床轉化率也是非常低的,平(píng)均在11%左右 。那麽到底是什麽原因導致了如此高比例的動物實驗結果無(wú)法實現在人類的臨床轉化呢?
1999年,美國麻省理工學院的機械工程師詹(zhān)姆斯·海伍德在得知(zhī)他的哥哥史蒂芬·海伍德被確診患有ALS,並無任何有(yǒu)效治療方(fāng)法後,與家人一起創立了一家非盈利性生物技術公司,即ALS 治療開(kāi)發研究所(suǒ) (ALS-TDI)。ALS-TDI成立後開展了一項旨在尋找SOD1*G93A轉基因小鼠實驗結果臨(lín)床轉化失敗原因的項目,即使用SOD1*G93A轉基因小鼠重(chóng)複已發表科研論文中的動物(wù)實驗,以找出其臨床轉化失敗的原因。
在(zài)ALS-TDI開展的重(chóng)複性實驗中,他們不僅嚴格執行盲法(fǎ)對照,而且對給藥組和對照組的動物進行了更為精細的分配和動物篩查以排除係(xì)統誤差。他們分組(zǔ)及實驗要求包括:
⑴ 年齡匹配;
⑵ 性別匹配;
⑶ 同窩匹配:即使用同一天出生的同一非轉基(jī)因母親和轉基因父親的後代進行分組,具(jù)體來說,治療(liáo)組中的每個雄性(和雌(cí)性)在對照組(zǔ)中都有一個同窩兄弟(和姐(jiě)妹);
⑷ 樣本量設定:每組使用動物數(shù)量為24隻(12雌,12雄);
⑸ 死因篩查:檢查記(jì)錄每一隻動物的死亡原因(yīn),排出非ALS致死個體;
⑹ 轉(zhuǎn)基因拷貝數監控:有研究證明SOD1*G93A轉基因小鼠在傳代過程中會出現轉基因拷貝數丟(diū)失的現象(xiàng),且低拷貝的轉基因小鼠的平均壽命會加長。
在這一嚴格實驗分組和動物篩查條件下(xià),ALS-TDI的科研人員(yuán)總(zǒng)共使用了5429隻SOD1*G93A轉基因小鼠測試了包括利魯唑在內的100多種(大部(bù)分已有論文發表並(bìng)證明可延長SOD1*G93A轉基因小鼠壽(shòu)命(mìng))候選化(huà)合物,卻沒有發現任一化合物表現出可延長SOD1*G93A轉基因小鼠壽命的(de)效果(圖三)。
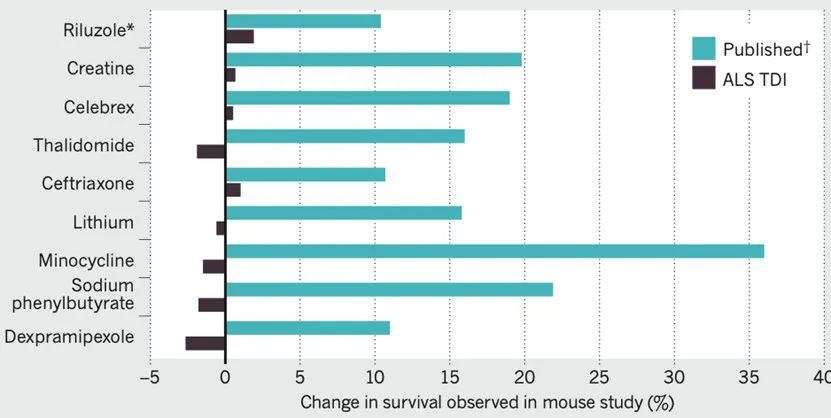
圖三:ALS-TDI以SOD1*G93A轉基因小(xiǎo)鼠開展的重(chóng)複實驗結果與已發表實驗結(jié)果對(duì)比[3]
為(wéi)找出導致那些已經發表(biǎo)實驗結(jié)果無法被(bèi)重複的原因,他們以在ALS-TDI開展(zhǎn)實驗中(zhōng)所(suǒ)使用的2000多隻對照小鼠作為研究對象,進行了計算機分組模(mó)擬實(shí)驗。由於這些小鼠從出生到死亡及死(sǐ)亡原因的(de)信息在ALS-TDI都有詳細的記錄,因此他們能夠以所有對照小(xiǎo)鼠為數據庫,分析前述重複實驗中設定的不同分組和動物篩查條件對實驗結果(guǒ)的(de)影響。即(jí)通過計算(suàn)機對這些沒有經過任何藥物處理(lǐ)的小鼠進行(háng)分組,將(jiāng)一組設為假定的實驗組,而另一組設為假定的對照組,然(rán)後依據已有的小鼠死亡時間(jiān)記錄,統計(jì)兩組小鼠之間是(shì)否存在顯著差異。經過多次重複,計算出現5%以上顯著差異的百分比。由於這些對照小鼠(shǔ)沒有接受過任何化合物處理,因此如果假定的實驗組和對(duì)照(zhào)組中出現了顯著性差異,那麽其來(lái)源應該是分組時的係統誤差。
結(jié)果顯示,在樣本量大小為4的計算機分組模擬對比實驗中,在隨機分組(zǔ)和不進行(háng)死因篩查及排除(chú)低轉基因拷貝(bèi)數個體條件下,兩組間出現顯著差異的可能性超過(guò)了50%。而隨機分組(zǔ)的同時(shí)進行死因篩查並排除(chú)低轉基因拷貝數個體和進行性別匹配的(de)分組條件下,樣本量為4的模擬(nǐ)分組實驗中也有30%的可能出(chū)現兩組死亡時間的顯著差異(圖四(sì))。隨著樣本量的增加,出現顯著性差異的可能(néng)性逐漸減少,但要實現低於5%(統計學上通常設置的顯著置信區間)的顯著性差異,樣本量要達到每組24隻動物。如果不做分組條件控製,即(jí)使樣本量到50隻也難以排除係統誤差。
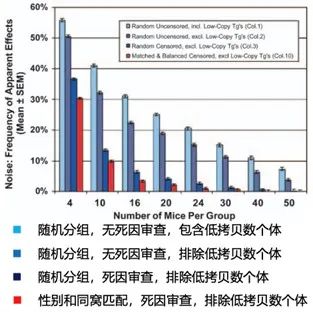
圖四:分組條件導(dǎo)致(zhì)的係統誤差[3]
ALS- TDI的這個計算機模擬實驗結果說明,前述那些已經發表的(de)基於SOD1*G93A轉基(jī)因小鼠(shǔ)實驗結果無法實現臨床轉化的真正原因極大可能源於其實驗設計的不合理。這些實驗因為沒有排除(chú)分組時的係統誤差而導致(zhì)了假陽性結果。這個研究也暴露(lù)了當下使用(yòng)實驗動物(wù)開展研究的諸多(duō)問題(tí),如盲目地追求(qiú)減少使(shǐ)用動物(wù)的數量;對所用(yòng)動物遺傳、微生物和繁殖等特(tè)性不了解;實驗過程中對動物關注不夠,不清楚動物發病(bìng)或死(sǐ)亡的真正(zhèng)原因等。這些問題不僅僅需要引起實驗動物從業人員(yuán)的注意,科研人員同樣需要給予(yǔ)關注。因為實驗設計不嚴謹導致的假陽性結果不僅是人力、物力和財力的(de)巨大浪費,也嚴重有違動物實驗倫理福利(lì),這樣的實驗不會帶來科學進步,且浪費了大(dà)量實驗動物的生命。比如在ALS-TDI開展的(de)無法重複出已發表結果的實驗中,那些已經發表的(de)工作累(lèi)計使用小鼠的數量就超過了18000隻。此外,在動物(wù)實驗倫理申請時常用替代、優化和減少(俗(sú)稱3R原(yuán)則)原則來指導倫理審查工作,有時為(wéi)了(le)滿足3R原(yuán)則中的“減少”原則,加上開展實驗成本的考慮,往往選擇使用最少的動物數量(比如多為每組6隻),但(dàn)從ALS-TDI的這個研究看,樣本量(liàng)過小,會導致係統誤差加大,因此極(jí)大可能出現假陽性結果。這個時(shí)候大家(jiā)或許忘了3R原則使用的(de)大前提是要能夠實現擬開展實驗的科學(xué)目標,如果單純為了“減少”而使用更少的實(shí)驗動物導致科學目標無(wú)法實現,那不是減少(shǎo),而是(shì)對動物(wù)生命的漠(mò)視。
參考文獻:
1.Rosen DR, Siddique T, Patterson D, Figlewicz DA, Sapp P, Hentati A, Donaldson D, Goto J, O'Regan JP, Deng HX, et al.: Mutations in Cu/Zn superoxide dismutase gene are associated with familial amyotrophic lateral sclerosis. Nature 1993, 362:59-62.
2.Tu PH, Raju P, Robinson KA, Gurney ME, Trojanowski JQ, Lee VM: Transgenic mice carrying a human mutant superoxide dismutase transgene develop neuronal cytoskeletal pathology resembling human amyotrophic lateral sclerosis lesions. Proc Natl Acad Sci U S A 1996, 93:3155-3160.
3.Scott S, Kranz JE, Cole J, Lincecum JM, Thompson K, Kelly N, Bostrom A, Theodoss J, Al-Nakhala BM, Vieira FG, et al: Design, power, and interpretation of studies in the standard murine model of ALS. Amyotroph Lateral Scler 2008, 9:4-15.
4.Fornai F, Longone P, Cafaro L, Kastsiuchenka O, Ferrucci M, Manca ML, Lazzeri G, Spalloni A, Bellio N, Lenzi P, et al: Lithium delays progression of amyotrophic lateral sclerosis. Proc Natl Acad Sci U S A 2008, 105:2052-2057.
5.Kola I, Landis J: Can the pharmaceutical industry reduce attrition rates? Nat Rev Drug Discov 2004, 3:711-715.
6.Hay M, Thomas DW, Craighead JL, Economides C, Rosenthal J: Clinical development success rates for investigational drugs. Nat Biotechnol 2014, 32:40-51.


