
-
2025-3-11
唐菖蒲伯克霍爾德氏菌
-
2025-3-4
動物皮(pí)膚活檢及其(qí)福利考量
-
2025-2-25
實驗大小鼠食物和飲水的限製
-
2025-2-18
猴B病毒新發感染案(àn)例(lì)帶來的啟示(shì)
-
2025-2-11
實驗動(dòng)物配方(fāng)飼料的種類
-
2025-1-21
大鼠麻醉指(zhǐ)導原則(zé)
-
2025-1-14
齧齒類實驗動物常見的鞭毛蟲
-
2025-1-7
獸醫隨筆:實驗動物營養需求及其影響(xiǎng)因素
-
2024-12-31
貓科(kē)動物(wù)的(de)新殺(shā)手
-
2024-12-24
犬骨髓穿刺(cì)抽吸技(jì)術
滴眼給藥毒(dú)性試驗2-藥物眼部暴露與安全性評價
在上一篇滴眼給藥毒性試驗1中,咱們一起了解了其目的與試驗設計(jì),今天咱們繼續,看看這篇(piān)綜述中關於滴(dī)眼給(gěi)藥的眼部暴露,以及局部和全身安全性評價的內容。
眼部暴露
滴眼給藥毒性試驗的供試品標準濃度從0.001%到10%(即0.01 mg/mL至100 mg/mL)不等。滴眼液(yè)滴入眼睛後會被淚(lèi)液稀(xī)釋,並在(zài)一定程度上受到淚膜的阻滯,尤其是對於蛋白結合率高的供試品。然而,眼表各組織(如結膜和角膜上(shàng)皮)的供試品(pǐn)濃度卻非常高。
相反(fǎn),房水的藥物生物利用度通常低於10%。已有多位(wèi)研究者探究了影響滴眼液吸收的因素。影響(xiǎng)眼滲透性的藥物化學(xué)特性包括:親水性或親脂(zhī)性、離子(zǐ)化或去離子化、分(fèn)子量、製劑中的供試品濃度以及製劑中(zhōng)的添加劑等。藥物滴入眼睛後會分布到各個(gè)部分。其分布(bù)途徑可簡單地分成兩種:(1)角膜途(tú)徑和(2)結膜/鞏膜途徑。
最近,有研究者從(cóng)視網膜/脈絡膜給藥的角度假設存在三(sān)種途徑:
(1)(經角膜)穿過玻璃體的途徑
(2)(經角膜)葡萄膜——鞏膜的(de)途徑
(3)(經鞏膜)眼周途徑。各藥物的分布取決於其理化性質,如圖1所示。
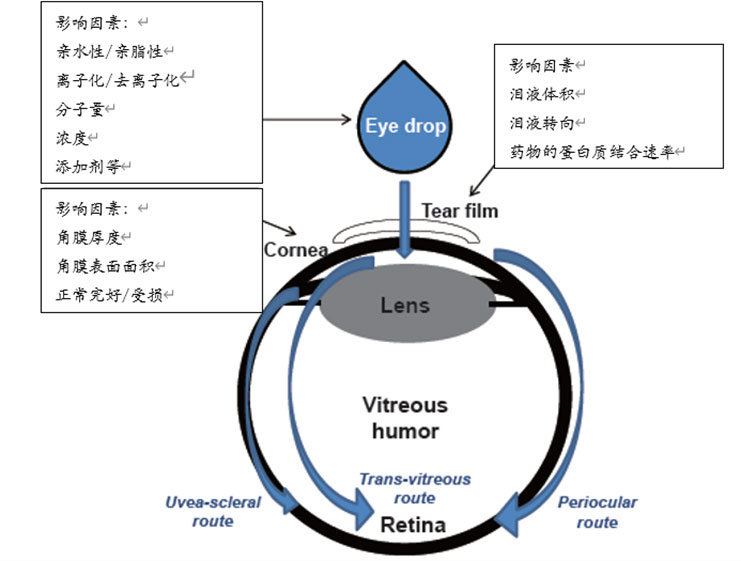
圖1 影響眼部藥物吸收的因(yīn)素
動物的生理條(tiáo)件可能會影響眼毒性(xìng)反應。由於藥(yào)物濃(nóng)度梯度限(xiàn)製了藥物的吸收,角膜滲透主(zhǔ)要取決於藥物濃度(dù)。因此(cǐ),如淚液體積發(fā)生變化,無論這種變化是否(fǒu)與供試品有關(如麻醉的影響),角膜對藥物(wù)的吸收速率都會改(gǎi)變。已知(zhī)眨眼會將藥物從眼表排出,這意味(wèi)著如眨眼頻率發(fā)生變化,眼部毒性反應的嚴重程度也可能會發生變化。此外,如角膜上皮不完整(如角膜損傷),親水性藥物更容易進入眼內。這表明,一旦角膜上(shàng)皮受(shòu)損,眼部供試品的暴露(lù)水平將提高,毒性(xìng)反應也(yě)會加(jiā)重。
最近已有多篇關(guān)於眼內轉運蛋白的文章發表。研究證實,角膜、虹膜-睫狀體和視網膜/脈絡膜等多個組織中存在轉運蛋白。Zhang等人(2008)通過比較不同物種(家兔、犬、食蟹猴和人類)不同眼組織中轉(zhuǎn)運蛋白基因表達水平(píng)的差異,發現人眼組織中的主要(yào)外排轉運蛋白(bái)是多藥耐(nài)藥相關蛋白1(MRP1),主要的攝取轉(zhuǎn)運蛋白是肽轉運蛋白1(PEPT1),以(yǐ)及有(yǒu)機陽離子轉運蛋白1(OCT1)、有機陽離子轉運蛋白新型1(OCTN1)和有(yǒu)機陽離子轉運(yùn)體(tǐ)新型2(OCTN2)。轉運蛋白對藥物的眼部藥(yào)代動力學和物種間特異性的影響有待進一步研究。
在眼睛滴入供試品後,眼後節(jiē)的暴露水(shuǐ)平(píng)遠低於眼前(qián)節。這是因為視網膜上,尤其是視(shì)網膜後部,存在(zài)多個解剖和功能結(jié)構,這些結構會阻礙(ài)供試品的進入。盡管(guǎn)如此,某些(xiē)滴眼液(如溴莫尼定、二氟潑尼酯和地塞(sāi)米鬆等)在滴眼(yǎn)後仍能在視網膜上發揮藥效。一項關於尼普地洛的研(yán)究(jiū)表明,局部滲透的主要路徑是藥物滴入眼睛後,從後節眼周(zhōu)組織逐步擴散,穿過鞏膜後部到達視網膜脈絡膜後(hòu)部。近(jìn)年來,眼後節(jiē)局(jú)部(bù)給藥藥物(wù)遞送係統正在研發中。在眼後節給藥(yào)藥物(wù)的研發過程中,眼後(hòu)節的安全性評估將變得更加重要。
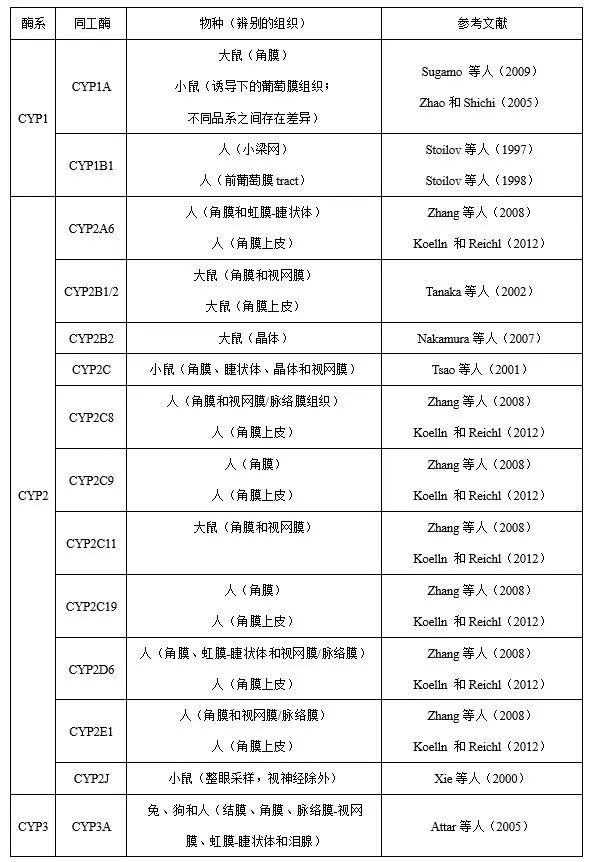
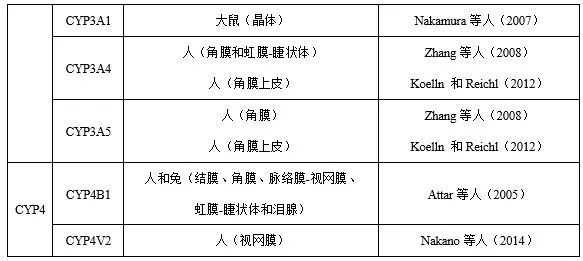
目前,已有(yǒu)多篇關於眼組織藥物代謝的文章發表。研究表明,眼組(zǔ)織中檢測(cè)到(dào)大(dà)量的細胞色素P450酶(CYP),見表1。然而,眼組織中這些酶的活性或基因表達水平遠低(dī)於參與藥物代謝的其他器官(如肝髒)的活性或水平。關於(yú)其他藥(yào)物代謝酶,Attar等(2005、2013)引入了氧化還原酶(如醛氧化酶、酮還原酶、環氧化酶(méi)、單(dān)胺氧化酶)、水(shuǐ)解酶(如氨肽酶、乙酰膽堿酯(zhǐ)酶、丁酰膽堿酯酶、羧化酯酶、磷酸酶、芳基磺化酶、N-乙酰-β-氨基葡萄糖苷酶、β-葡萄糖醛酸酶)和結合酶(如芳胺乙酰轉移酶和穀(gǔ)胱甘肽S-轉(zhuǎn)移酶)。其中部(bù)分(fèn)酶參與局部給藥的藥物代謝。然而(ér),關於不同物種及不同眼組織(zhī)中酶的差異(yì),相(xiàng)關資料仍然很少。
表1 眼組(zǔ)織細胞色素P450酶係
與黑色素的親和性是影響眼內藥物毒理特征的另一重要因素。有研究者報告稱,有色(sè)素動物的藥效比白化動(dòng)物的(de)藥效(xiào)更輕微。如藥物(wù)與黑色素(sù)結合,黑色素(sù)的含量可能會降低靶位點的自(zì)由藥物濃度,從而導致藥效減弱。反(fǎn)過來,藥物與黑色素結合後可能會蓄積(jī),然後逐(zhú)漸釋放,從而延長藥效(即使(shǐ)是在停藥後)。Leblanc等人(1998)認為,藥物本身與黑色素結合並不(bú)會(huì)影響眼部毒性(xìng)反應。因此,能與黑色素結合的(de)藥物的眼部毒性特征取決於藥物(wù)的毒性、與黑色素的結合(hé)方式和接觸時間(包括(kuò)停藥期)。
眼毒性和安全性評估
對於滴眼液(yè)製劑形(xíng)式的供試品,其毒性可分為原發性毒性、脫靶毒性和化學品相關效應。由於(yú)局部給藥位點處的供試品濃度較高,毒性反應主要發生在眼前節。因此,毒性反應最常見於角膜、結膜、虹膜(mó)和眼周組織(zhī)/器官(如眼瞼、皮膚(fū)和淚腺(xiàn))。實際(jì)上,隨著多款眼表滴眼液的上市,已有多起不良事件被(bèi)報道。
角膜、結膜和眼瞼
基於(yú)預試驗(如體外細胞毒性試驗(yàn)),從諸多細胞毒性較弱(ruò)的供試品中選出適合的供試品,開展滴眼給藥毒性試驗,以(yǐ)支持臨床試驗。此外,供(gòng)試品的製劑也會根據臨床(chuáng)人體試驗所用製劑進行調(diào)整。因此(cǐ),預計在滴眼給(gěi)藥毒性(xìng)試(shì)驗中不會出現化(huà)學燒傷或化學腐蝕等明顯的毒性反應。
充血是OITSs和臨床局部給藥中常見的反(fǎn)應。如供試品具有擴張血管(guǎn)的效果,充(chōng)血通常(cháng)是暫時的,且不(bú)伴隨組織(zhī)病理學(xué)變化。然而,如充血是由組織損傷引起,則可伴(bàn)隨水腫和炎症。
角膜混濁在毒理學上具有重要(yào)意義,因其會幹擾視力。因此(cǐ),試驗應設置恢複期,以探究(jiū)角膜混濁的可逆性。角膜(mó)混濁的可逆性可因受損位置而有(yǒu)所不同。由於兔和人類的角膜(mó)上皮細胞在一周內能再生,如損(sǔn)傷區域僅限於角膜上皮和角膜中心,角膜混濁很可能會消失。相反,如角膜上皮的幹細胞(如角(jiǎo)膜緣)受損,角膜混濁可能難以複(fù)原。
由於角膜內皮在維持角(jiǎo)膜(mó)內部(bù)液體平衡中發揮重要作用,因(yīn)此角膜內皮損傷後,常發生基質水腫(zhǒng)。角膜(mó)基質出現水(shuǐ)腫、細(xì)胞浸潤以及供試品或礦物質元素沉積,都可能導致角膜混濁。兔的角(jiǎo)膜上皮具有再生能(néng)力,但成年靈長類動物或犬的角膜內(nèi)皮卻沒有這種再生(shēng)能力。因(yīn)此,應認真(zhēn)評估兔角膜內皮(pí)的可逆性,並探究其與人類角(jiǎo)膜上皮可逆性的相關性。無論如何,一(yī)旦(dàn)基質受損,由於(yú)基質重塑速度緩慢,角膜透明度的恢複時間會相對較長。在這(zhè)種情況下,纖維組織可能(néng)會修複基質(zhì)損傷,但角膜透(tòu)明度可能無法(fǎ)完全恢(huī)複。
滴(dī)眼液通常會標明與過敏相(xiàng)關的注意事項。然而(ér),判斷滴眼給(gěi)藥毒性(xìng)試驗中眼表炎症是否與過敏相關通常非常困難。可以利用(yòng)其他非(fēi)臨床手段評估致敏風險,如小鼠局部淋巴結試驗(OECD,2010)。
已(yǐ)知口服陽離子兩親性藥物會引起動物和人類角膜磷脂沉積。Bockhardt等人(1978)報告(gào)了胺碘酮脂滴(dī)眼誘導(dǎo)大鼠類脂沉積。有研究者證實,給予兔滴眼液會導致角(jiǎo)膜磷(lín)脂沉積。如果磷脂沉積與角膜混濁無關,且一直在組織病(bìng)理學(xué)評估範圍內,那麽此鏡檢(jiǎn)發現的毒理學(xué)意義可能不大。胺碘酮誘導的人體角膜磷(lín)脂沉積是可逆的,且對視力的損(sǔn)害很小。
淚液(yè)分泌減少會導致幹眼症。已知(zhī)幾種滴眼液會引起(qǐ)淚液係統(tǒng)功能(néng)失調。因此,在評估角膜毒性反應時,應考慮淚膜的(de)完整性。
葡萄(táo)膜(mó)
眼壓會受到原發性藥理作用(如青光眼治療藥物)、脫靶性藥理作用、炎(yán)症引起的組織功能(néng)紊亂或損傷的影響。眼壓持(chí)續升高可能會導致青光眼,進而引發功能性眼損傷,甚(shèn)至視力(lì)損傷。
藥物(wù)的原發性或脫(tuō)靶性藥(yào)理作用(yòng)能引起散瞳或縮瞳,但這些效應通常是暫時的。散瞳或限製瞳孔收縮(suō)的藥物會(huì)導致前房(fáng)變淺和房角變窄,這些結構性變化可(kě)能會導致眼(yǎn)壓升高。有研究者報告稱,皮質類固醇會誘(yòu)導人(rén)類眼壓升高,但這種現象在(zài)動物(wù)身上並未重現。
某些(xiē)滴眼液會導致虹膜變色。有研究者(zhě)報告稱,治(zhì)療青光(guāng)眼的β阻斷劑(jì)左布諾洛爾(ěr)會引起人類虹膜褪色。Schafer和Render(2013a)認為,炎(yán)症可能會導致葡萄膜褪色。另一方麵,類前列腺素會促進黑色素合成,導致虹膜色素沉著。在患者身上,這種色素沉著通常是永久性的。
晶狀(zhuàng)體
晶狀體的前端正對著眼房,眼房內(nèi)充盈著房水(shuǐ)。這(zhè)種(zhǒng)結(jié)構使晶狀體上皮能直接接觸到(dào)眼房內的(de)藥物。有研究者報告稱,人類晶狀體混(hún)濁可能是藥物局部(bù)應用引起(qǐ)的,例如抗(kàng)膽堿酯酶、毛果芸香堿(jiǎn)和乙酰膽(dǎn)堿。在動物實驗中,發現晶(jīng)狀體(tǐ)混濁是(shì)由多(duō)重機製引發的,包括糖、蛋白質、脂質和電解質代謝異常。人類和動物的部分晶(jīng)狀體混濁是暫時性的,但受損晶狀體(tǐ)組織的修複速(sù)度(dù)非常緩慢。Schafer 和 Render(2013b)認為,糖(táng)皮質(zhì)激素誘導的人類白內障難以(yǐ)在動物模型中複現(xiàn)。
視網膜
許多藥(yào)物和(hé)化(huà)學品可引起各種形式的視網膜毒(dú)性。如(rú)藥物通過係統給藥(yào),視網膜(mó)毒性在(zài)非臨床試驗和臨床試驗中都較為(wéi)常見;而局部給藥(yào)則較少出現毒性反應。這很可能是由於局部給藥時藥物的生物利用度較低(dī),尤其(qí)是眼後節,包括視網膜在內的生物利用度更低。然而,如上所述,有報告稱某些滴眼液在眼後節也能發揮藥理作用。因此,對視網膜進行(háng)OITSs眼科檢查變得尤為重要,包括使用成像(xiàng)技術檢測輕微的視網膜變化。
特異質藥物不良反應
特異質藥物不良反應(IDRs)被認為是可能(néng)致命的人(rén)體副作用,主要影響皮膚、肝髒和骨髓。有研究人員認為這些反應(yīng)是(shì)由免疫介導的。根據George等人(2014)的表述,局部給藥時出現Stevens-Johnson綜合征(SJS)和中(zhōng)毒性表皮壞死鬆解症(TEN)的情況非常罕見。然而,已有案例報告顯示,多佐胺/噻嗎洛爾/拉(lā)坦(tǎn)前列(liè)素滴眼液可引起TEN(弗洛雷斯等人(rén),2005),而(ér)磺胺甲惡唑滴眼(yǎn)液則可引發Stevens-Johnson綜合征。因(yīn)此,在未來的非(fēi)臨床試(shì)驗中,應考慮對特異質藥物不良反應進(jìn)行安全性評估。
局部和係(xì)統未觀察到有害作用水平
在(zài)滴眼給藥的毒性試驗中,局部和係統未觀察到有害作用水平應分(fèn)別定義。Lewis等人(rén)(2002)建議,在局部給藥試(shì)驗中,應建立兩(liǎng)種未觀察到有(yǒu)害作用(yòng)水平:一種基於局部(給(gěi)藥部位)藥效,另一種(zhǒng)基於(yú)係統藥效。OITSs的局(jú)部毒性反應(yīng)和係統毒性反應通常不會相互影響(xiǎng)。然而,如果動物狀況不(bú)佳,係統毒(dú)性可(kě)能會影(yǐng)響眼科檢查結果。
計算機模擬預測眼部暴露量和眼毒性風險評估(gū)
測量人體眼組織的藥物暴露水平是不現實的。即使能測量(liàng)實驗動物眼組(zǔ)織的藥代動力學參數(shù),也需要大量動物才(cái)能(néng)進行全麵分析。計算機(jī)模(mó)擬的最新進展或許能夠解決這一困(kùn)境。例如,Tojo(2004)建立了眼部給藥的(de)藥(yào)代動力學模型。有研究者報告使用計算(suàn)機模擬了兔子(zǐ)滴眼給藥後眼(yǎn)前節組織的藥物滲透情況。此外(wài),Ueda等人(rén)(2010)建(jiàn)立了正常眼和患病眼中抗菌(jun1)藥物(wù)的眼部(bù)擴散模型。這些模(mó)擬模型和(hé)計算機預測有助於估算人體(tǐ)和動物的眼(yǎn)部暴露量,並為未來技術發展提供了挑戰和機(jī)遇。
滴眼給藥(yào)毒性試驗的係統毒性
全身器官(guān)檢查OITSs的係統毒性評估(gū)與通過係統給藥的一般毒性試驗的(de)係統(tǒng)毒(dú)性評估基本(běn)一致(zhì)。Weir和Wilson(2013)總(zǒng)結了(le)眼毒性試驗(yàn)的係統終點,具體檢查項目包括:臨床觀察、體重、攝食、臨(lín)床(chuáng)病(bìng)理、剖檢、髒器稱重、組織病理學、毒代動(dòng)力學(TK)和免疫原性(生物學)。基於既往的知識和經驗,活體階段的係統檢查(不包括前(qián)章所述的眼科檢查)如表2所示。其中,心電圖和血壓測量是猴和犬係統給藥的一般毒性試驗的常規檢查。由於滴眼(yǎn)液(yè)的副作用常見於心血管係統,因此OITSs也需要進(jìn)行相關參(cān)數的檢查。
表2 滴眼給藥毒性試(shì)驗中活體階段的係統檢查(除眼科檢查外)

與係統給藥的一般毒性試驗類似,在滴眼給藥毒性試驗(yàn)中也會對(duì)全身器官進(jìn)行組織病理學檢查,這對評估全身器官的毒性(xìng)具有重要意義(yì)。然而,如係統給藥(yào)的單個(gè)毒性試驗已確定未觀察(chá)到有害作用水平(NOAEL),且藥(yào)代動力(lì)學(TK)數據有(yǒu)效,那在滴(dī)眼(yǎn)給藥毒性試驗(yàn)中對全身器官進行組織病理學檢查可能意義不大。
毒性相關的係統暴露量的考量
與係統給藥的藥物相比,滴眼液的係統暴露水平相對較低(dī)。舉例來說,若雙(shuāng)眼每天滴入(rù)3次1%的滴眼液(假(jiǎ)設每滴體(tǐ)積為40 µL,體重(chóng)60 kg),可算出劑量水平為0.04 mg/kg/day。滴眼液的係統生物(wù)利用度通常高於(yú)75%,或20%至100%不等(děng)。相較於其眼內生物利用度,係統生物利用度相對較高。絕大部分滴眼液會流入鼻淚管並粘附(fù)在鼻黏膜上。在這(zhè)個過程中,滴眼液被吸收並進入係統循環。Lee等人(1993)報告稱,至少50%的藥物通過鼻(bí)黏膜經係統吸收進入血液。因此,眼科滴眼(yǎn)藥物的(de)藥代動(dòng)力學與靜脈注射藥(yào)物的藥代動力學相似,兩者都較少受到首過效(xiào)應的影響。一項使用噻(sāi)嗎(ma)洛爾的研究表明,人體靜脈注射和滴眼給藥的係統生物利用度和心肺效應相似。
毒(dú)代動力學在評估滴眼給藥毒性試驗的係統毒性方麵非常重(chóng)要。此外,在單側滴眼給藥時,TK數據有助於解釋對照眼(yǎn)的眼科檢查結果(guǒ)。目前,藥物濃度檢測的生物分析技術正不(bú)斷發(fā)展,能夠檢測到10 pg/mL甚至更(gèng)低(dī)的藥物(wù)濃度。這項技術的進步有助於更準確地評估OITSs和人體臨床試驗的藥代動力學特征,從而確定係統毒性(xìng)的安全邊際。
係統毒性反應和安全性評估
在滴眼液的臨床和非臨(lín)床試驗中,係統毒性(xìng)反應和副作用都非常(cháng)罕見(jiàn)。青光眼治療藥物引起的係統副作用主要影響心血管係統和中樞(shū)神經係統。因為滴(dī)眼液的劑量水平並不會根據受試者的體型而進行調整,所以體型(xíng)較(jiào)小的(de)人群(如兒童)出現係統副作用的風險相對(duì)較高(gāo)。此前(qián)已有多起滴眼液誘導兒童產生係統副作用的案例,例如阿托品、環(huán)戊酮和散瞳劑。
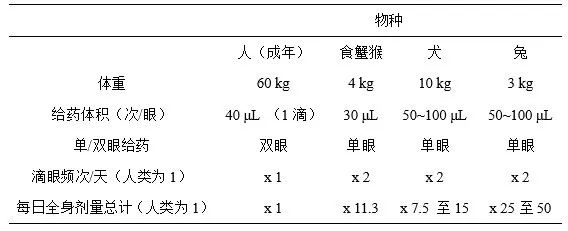
在(zài)眼科滴眼給藥(yào)毒性試驗(yàn)(OIITSs)中,係統劑量水平(píng)/體重遠遠(yuǎn)高於(yú)臨床試驗,這是因為所用的猴和兔的體(tǐ)重約為(wéi)3至4 kg。即使所用製劑的(de)藥物濃度相同(表3),猴和兔的日用係(xì)統劑量是人體的7.5至(zhì)50倍。如果提高藥物濃(nóng)度或增加給藥頻次,OIITSs的係(xì)統劑量水平將會與ICH M3指導原則(ICH, 2009)建議的(de)最高劑量水平(意味著暴露量是臨床劑(jì)量的50倍)持平。因此,在某些情況(kuàng)下,OIITSs適用於評估(gū)人體臨床試驗所(suǒ)用藥物的係統毒性(xìng)反應。總體而言,如在OIITSs中增加係統毒性(xìng)反應評估和係統(tǒng)毒代動力學(TK)評估,非臨床試驗就無需包(bāo)括單獨的係統毒性試驗。這種做法符合動物倫理委員會提出的3R原則(zé)(ILAR, 2011)。然(rán)而,關於是(shì)否需開展單獨的毒性試驗以評(píng)估係統毒性反(fǎn)應(yīng)的合理性,仍需進一步討論。
表3 臨床人體試(shì)驗和滴眼給(gěi)藥毒性試驗的相(xiàng)對係統劑量水平
結論
本篇綜述旨在在介紹滴眼給藥毒性試驗,引(yǐn)起研究(jiū)人員對這類特殊性試驗(yàn)某些要點的關注。滴眼給藥毒(dú)性試驗的特點之(zhī)一(yī)在於眼球直接給藥。在開展此類試(shì)驗時,毒理(lǐ)學家需認真設計試驗(yàn),製(zhì)定安全性評價策略,將滴眼液的所有特征納入到考慮範圍內。


